Лечение гастроэзофагеальной рефлюксной болезни. Гэрб – терапевтическое лечение
Catad_tema Изжога и ГЭРБ - статьи
Гастроэзофагеальная рефлюксная болезнь: диагностика, терапия и профилактика
А. В. Калинин
Государственный институт усовершенствования врачей МО РФ, Москва
РЕФЕРАТ
Гастроэзофагеальная рефлюксная болезнь: диагностика, терапия и профилактика
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) относится к частым заболеваниям. Еще сравнительно недавно ГЭРБ представлялась практическим врачам безобидным заболеванием с характерным симптомом - изжогой. В последнее десятилетие к ГЭРБ находится в зоне повышенного внимания в связи с отчетливой тенденцией к увеличению частоты тяжелых рефлюкс-эзо-фагитов и учащением рака дистальных отделов пищевода на фоне «пищевода Баррета». Установленная связь с ГЭРБ легочных заболеваний, в частности, бронхиальной астмы, позволяет по-новому подойти к их лечению. Принятие новой классификация рефлюкс-эзофагита способствовало унифициации эндоскопических, заключений. Внедрение суточной рН-метрии позволило диагностировать заболевание еще на эндоскопически негативной стадии. Широкое использование в клинической практике новых лекарственных препаратов (блокаторы Н 2 -рецепторов, ИПП, прокинетики) существенно расширило возможности лечения ГЭРБ, в т.ч. и при ее тяжелом течении. В качестве перспективного средства лечения и профилактики ГЭРБ рассматривается чистый S-изомер омепразола - эзомепразол (Нексиум).
В последнее десятилетие гастроэзофагеальная рефлюксная болезнь (ГЭРБ) привлекает к себе повышенное внимание, что связано со следующими обстоятельствами. В развитых странах мира наблюдается отчетливая тенденция к увеличению частоты ГЭРБ. Среди взрослого населения Европы и США изжога - кардинальный симптом ГЭРБ - встречается у 20-40%. Значение ГЭРБ определяется не только ее распространенностью, но и утяжелением течения. За последние десять лет в 2-3 раза чаще стали наблюдаться тяжелые рефлюкс-эзофагиты (РЭ). У 10-20% больных РЭ развивается патологическое состояние, описываемое как «пищевод Баррета» (ПБ) и являющееся предраковым заболеванием. Установлено также, что ГЭРБ занимает важное место в генезе ряда ЛОР и легочных заболеваний .
Существенный прогресс достигнут в диагностике и лечении ГЭРБ. Внедрение суточной рН-метрии позволило диагностировать заболевание еще на эндоскопически негативной стадии. Широкое использование в клинической практике новых лекарственных препаратов (блокаторы Н2-ренепторов, ингибиторы протонной помпы -ИПП, прокинетики) существенно расширило возможности лечения даже тяжелых форм ГЭРБ. Выработаны четкие показания к хирургическому лечению РЭ .
В то же время практические врачи и сами пациенты недооценивают значения этого заболевания. Больные в большинстве случаев поздно обращаются к врачу за медицинской помощью и даже при выраженных симптомах лечатся самостоятельно. Врачи, в свою очередь, плохо осведомлены о данном заболевании, недооценивают его последствия, нерационально проводят терапию РЭ. Крайне редко диагностируется такое серьезное осложнение, как ПБ.
Определение понятия «гастроэзофагеальная рефлюксная болезнь»
Попытки определения понятия «гастроэзофагеальная рефлюксная болезнь» сталкиваются со значительными трудностями:
- у практически здоровых лиц наблюдаются забросы желудочного содержимого в пищевод;
- достаточно продолжительное закисление дистального отдела пищевода может не сопровождаться клиническими симптомами и морфологическими признаками эзофагита;
- нередко при выраженных симптомах ГЭРБ отсутствуют воспалительные изменения в пищеводе.
Как самостоятельная нозологическая единица ГЭРБ официально получила признание в материалах по диагностике и лечению этого заболевания, принятых в октябре 1997 г. на междисциплинарном конгрессе гастроэнтерологов и эндоскопистов в г.Генвале (Бельгия). Было предложено выделять эндоскопически позитивную и эндоскопически негативную ГЭРБ. Последнее определение распространяется на те случаи, когда у пациента с проявлениями заболевания, отвечающего клиническим критериям ГЭРБ, отсутствуют повреждения слизистой пищевода. Таким образом, ГЭРБ не синоним рефлюкс-эзофагита, понятие это более широкое и включает в себя как формы с повреждением слизистой оболочки пищевода, так и случаи (более 70%) с типичными симптомами ГЭРБ, при которых при эндоскопическом исследовании видимые изменения слизистой оболочки пищевода отсутствуют.
Термином ГЭРБ большинство клиницистов и исследователей обозначают хроническое рецидивирующее заболевание, обусловленное спонтанным, регулярно повторяющимся ретроградным поступлением в пищевод желудочного и/или дуоденального содержимого, приводящим к повреждению дистального отдела пищевода и/или появлению характерных симптомов (изжога, ретростернальные боли, дисфагия).
Эпидемиология
Истинная распространенность ГЭРБ мало изучена. Это связано с большой вариабельностью клинических проявлений - от эпизодически возникающих изжог, при которых больные редко обращаются к врачу, до ярких признаков осложненного РЭ, требующего госпитального лечения .
Как уже отмечалось, среди взрослого населения Европы и США изжога, кардинальный симптом ГЭРБ, встречается у 20-40% популяции, однако только 2% лечатся по поводу РЭ. РЭ выявляется у 6-12% лиц, которым проводится эндоскопическое исследование.
Этиология и патогенез
ГЭРБ - многофакторное заболевание. Принято выделять ряд предрасполагающих к его развитию факторов: стресс; работа, связанная с наклонным положением туловища, ожирение, беременность, курение, хиатальная грыжа, некоторые лекарственные средства (антагонисты кальция, антихолинергические препараты, B-адреноблокаторы и др.), факторы питания (жир, шоколад, кофе, фруктовые соки, алкоголь, острая пища).
Непосредственной причиной РЭ является длительный контакт желудочного (соляная кислота, пепсин) или дуоденального (желчные кислоты, лизолецитин) содержимого со слизистой оболочкой пищевода.
Выделяют следующие причины, приводящие к развитию ГЭРБ:
- недостаточность запирательного механизма кардии;
- рефлюкс желудочного и дуоденального содержимого в пищевод;
- снижение пищеводного клиренса;
- уменьшение резистентности слизистой оболочки пищевода.
Недостаточность запирательного механизма кардии.
Поскольку давление в желудке выше, чем в грудной полости, рефлюкс желудочного содержимого в пищевод должен был бы быть явлением постоянным. Однако благодаря запирательному механизму кардии он возникает редко, на короткое время (менее 5 мин), и вследствие этого не рассматривается как патология. Нормальные показатели рН в пищеводе - 5,5-7,0. Пищеводный рефлюкс следует считать патологическим, если общее число его эпизодов в течение суток превышает 50 или общее время снижения внут-рипищеводного рН <4 в течение суток превышает 4 ч.
К механизмам, поддерживающим состоятельность функции пищеводно-желудочного перехода (запирательный механизм кардии), относятся:
- нижний пищеводный сфинктер (НПС);
- диафрагмально-пищеводная связка;
- слизистая «розетка»;
- острый угол Гиса, образующий клапан Губарева;
- внутрибрюшное расположение нижнего пищеводного сфинктера;
- круговые мышечные волокна кардиального отдела желудка.
Возникновение желудочно-пищеводного рефлюкса есть результат относительной или абсолютной недостаточности запирательного механизма кардии. К относительной недостаточности кардии приводит значительный рост интрагастрального давления при сохраненном запирательном механизме. Так, например, интенсивное сокращение антрального отдела желудка способно вызвать гастроэзофагеальный рефлюкс даже у лиц с нормальной функцией нижнего пищеводного сфинктера. Относительная недостаточность кардиаль-ного затвора встречается, по данным А.Л. Гребенева и В.М. Нечаева (1995), у 9-13% больных с ГЭРБ. Гораздо чаще имеет место абсолютная кардиальная недостаточность, связанная с нарушением запирательного механизма кардии.
Главная роль в запирательном механизме отводится состоянию НПС. У здоровых лиц давление в данной зоне составляет 20,8+3 мм рт. ст. У больных ГЭРБ оно снижается до 8,9+2,3 мм рт. ст.
Тонус НПС находится под воздействием значительного числа экзогенных и эндогенных факторов. Давление в нем снижается под влиянием ряда гастроинтестинальных гормонов: глюкогона, соматостатина, холецистокинина, секретина, вазоактивного интестинального пептида, энкефалинов. Некоторые из широко применяемых лекарственных препаратов также оказывают депрессивное воздействие на запирательную функцию кардии (холинергические вещества, седативные и снотворные средства, b-адреноблокаторы, нитраты и др.). Наконец, тонус НПС снижают некоторые продукты питания: жиры, шоколад, цитрусовые, томаты, а также алкоголь и табак.
Прямое поражение мышечной ткани НПС (хирургические вмешательства, длительное присутствие назогастрального зонда, бужирование пищевода, склеродермия) также может приводить к гастроэзофагеальному рефлюксу.
Другим важным элементом запирательного механизма кардии является угол Гиса. Он представляет собой угол перехода одной боковой стенки пищевода в большую кривизну желудка, тогда как другая боковая стенка плавно переходит в малую кривизну. Воздушный пузырь желудка и внутрижелудочное давление способствуют тому, что складки слизистой оболочки, образующей угол Гиса, плотно прилегают к правой стенке, предотвращая тем самым забрасывание содержимого желудка в пищевод (клапан Губарева).
Часто ретроградное попадание желудочного или дуоденального содержимого в пищевод наблюдается у больных с хиатальной грыжей. Она грыжа обнаруживается у 50% обследуемых в возрасте старше 50 лет, причем у 63-84% таких пациентов эндоскопически определяются признаки РЭ.
Рефлюкс при грыже пищеводного отверстия диафрагмы объясняется рядом причин:
- дистопия желудка в грудную полость приводит к исчезновению угла Гиса и нарушению клапанного механизма кардии (клапан Губарева);
- наличие грыжи нивелирует запирающее действие диафрагмальных ножек в отношении кардии;
- локализация НПС в брюшной полости предполагает воздействие на него положительного внутрибрюшного давления, которое в значительной степени потенцирует запирательный механизм кардии.
Роль рефлюкса желудочного и дуоденального содержимого при ГЭРБ.
Прослеживается положительная связь между вероятностью РЭ и уровнем закисления пищевода. Исследования на животных продемонстрировали повреждающее действие ионов водорода и пепсина, а также желчных кислот и трипсина на защитный слизистый барьер пищевода. Однако ведущая роль отводится не абсолютным показателям агрессивных компонентов желудочного и дуоденального содержимого, попадающих в пищевод, а снижению клиренса и резистентности слизистой оболочки пищевода.
Клиренс и резистентность слизистой оболочки пищевода.
Пищевод снабжен эффективным механизмом, позволяющим устранять сдвиги внутрипищеводного уровня рН в кислую сторону. Этот защитный механизм обозначается как пищеводный клиренс и определяется как скорость убывания химического раздражителя из полости пищевода. Эзофагеальный клиренс обеспечивается за счет активной перистальтики органа, а также ощелачивающими свойствами слюны и слизи. При ГЭРБ происходит замедление пищеводного клиренса, связанное прежде всего с ослаблением перистальтики пищевода и антирефлюксного барьера.
Резистентность слизистой оболочки пищевода обусловлена преэпителиальным, эпителиальным и постэпителиальным факторами. Повреждение эпителия начинается, когда ионы водорода и пепсин или желчные кислоты преодолевают водный слой, омывающий слизистую оболочку, преэпителиальный защитный слой слизи и активную бикарбонатную секрецию. Клеточная резистентность к ионам водорода зависит от нормального уровня внутриклеточной рН (7,3-7,4). Некроз возникает, когда этот механизм исчерпывается, и происходит гибель клеток вследствие их резкого закисления. Противостоит образованию небольших поверхностных изъязвлений увеличение клеточного оборота за счет усиленного размножения базальных клеток слизистой оболочки пищевода. Эффективным постэпителиальным защитным механизмом от кислотной агрессии является кровоснабжение слизистой оболочки.
Классификация
Согласно Международной классификации болезней 10 пересмотра, ГЭРБ относится к рубрике К21 и подразделяется на ГЭРБ с эзофагитом (К21.0) и без эзофагита (К21.1).
Для классификации ГЭРБ принципиальное значение имеет степень выраженности РЭ.
В 1994 г. в Лос-Анджелесе была принята классификация, в которой выделены эндоскопически позитивная и эндоскопически негативная стадии ГЭРБ. Термин «повреждение слизистой оболочки пищевода» пришел на смену понятиям «ульцерация» и «эрозия». Одним из преимуществ этой классификации является ее относительная простота при использовании в повседневной практике. Лос-анджелесскую классификацию РЭ было рекомендовано использовать при оценке результатов эндоскопического исследования (табл. 1).
Характеристику осложнений РЭ (язвы, стриктуры, метаплазия) лос-анджелесская классификация не предусматривает. В настоящее время более широко используется классификация Savary-Miller (1978) в модификации Carisson и соавт. (1996), представленная в таблице 2.
Представляет интерес новая клинико-эндоскопическая классификация, которая подразделяет ГЭРБ на три группы:
- неэрозивная, наиболее частая форма (60% всех случаев ГЭРБ), к которой относят ГЭРБ без признаков эзофа-гита и катаральный РЭ;
- эрозивно-язвенная форма (34%), включая ее осложнения: язва и стриктура пищевода;
- пищевод Баррета (6%) - метаплазия многослойного плоского эпителия на цилиндрический в дистальном отделе как следствие ГЭРБ (выделение этой ПБ связано с тем, что эта форма метаплазии рассматривается как предраковое состояние).
Клиника и диагностика
Первый этап диагностики - опрос больного. Среди симптомов ГЭРБ основное значение имеют изжога, кислая отрыжка, ощущение жжения в эпигаст-рии и за грудиной, которые чаще возникают после еды, при наклоне туловища вперед или в ночное время. Вторым по частоте проявлением данного заболевания является ретростерналъная боль, которая иррадиирует в межлопаточную область, шею, нижнюю челюсть, левую половину грудной клетки и может имитировать стенокардию. Для дифференциальной диагностики генеза болей важно, что провоцирует и купирует их. Для эзофагеальных болей характерна связь с приемом пищи, положением тела и купирование приемом щелочных минеральных вод и соды.
К внепищеводным проявлениям заболевания относят легочные (кашель, одышка, чаще возникающие в положении лежа), отоларингологические (охриплость голоса, сухость в горле) и желудочные (быстрое насыщение, вздутие, тошнота, рвота) симптомы.
При рентгенологическом исследовании пищевода удается зафиксировать попадание контраста из желудка в пищевод, обнаружить грыжу пищеводного отверстия диафрагмы, язву, стриктуры и опухоль пищевода.
Для лучшего выявления желудочно-пищеводного рефлюкса и грыжи пищеводного отверстия диафрагмы необходимо провести полипозиционное исследование при наклонах пациента кпереди с натуживанием и покашливанием, а также лежа на спине при опускании головного конца туловища.
Более надежным методом обнаружения гастроэзофагеального заброса является суточная (24-часовая) рН-метрия пищевода, позволяющая оценить частоту, продолжительность и выраженность рефлюкса, влияние на него положения тела, приема пищи и лекарственных средств. Исследование суточных изменений рН и пищеводного клиренса позволяет выявить случаи рефлюкса до развития эзофагита.
В последние годы для оценки эзофагеального клиренса применяется сцинтиграфия пищевода с радиоактивным изотопом технеция. Задержка принятого изотопа в пищеводе более чем на 10 мин указывает на замедление эзофагеального клиренса.
Эзофагоманометрия - измерение давления в пищеводе с помощью специальных баллонных зондов - может дать ценные сведения о понижении давления в зоне НПС, нарушениях перистальтики и тонуса пищевода. Однако в клинической практике этот метод применяется редко.
Основным методом диагностики РЭ является эндоскопический. С помощью эндоскопии можно получить подтверждение наличия РЭ и оценить степень его тяжести, провести контроль заживления повреждений слизистой оболочки пищевода.
Биопсия пищевода с последующим гистологическим исследованием производится в основном для подтверждения наличия ПБ при характерной эндоскопической картине, поскольку верифицировать ПБ можно только гистологически.
Осложнения рефлюкс-эзофагита
Пептические язвы пищевода наблюдаются у 2-7% больных ГЭРБ, в 15% случа ев язвы осложняются перфорацией, чаше всего в средостение. Острые и хронические кровопотери различной степени встречаются практически у всех пациентов с пептическими язвами пищевода, причем сильные кровотечения отмечаются у половины из них.
Таблица 1.
Лосанджелесская классификация РЭ
|
Степень тяжести РЭ |
Характеристика изменений |
| Степень А | Одно или несколько повреждений слизистой оболочки пищевода длиной не более 5 мм, ограниченные одной складкой слизистой оболочки |
| Степень В | Одно или несколько повреждений слизистой оболочки пищевода длиной более 5 мм, ограниченные складками слизистой оболочки, причем повреждения не распространяются между двумя складками |
| Степень С | Одно или несколько повреждений слизистой оболочки пищевода длиной более 5 мм, ограниченные складками слизистой оболочки, причем повреждения распространяются между двумя складками, но занимают менее 75% окружности пищевода |
| Степень D | Повреждения слизистой оболочки пищевода, охватывающие 75% и более его окружности |
Таблица 2.
Классификация РЭ по Savary-Miller в модификации Carisson и соавт.
Стенозирование пищевода придает заболеванию более стойкий характер: прогрессирует дисфагия, снижается масса тела. Стриктуры пищевода встречаются примерно у 10% больных ГЭРБ. Клинические симптомы стеноза (дисфагия) появляются при сужении просвета пищевода до 2 см.
К серьезному осложнению ГЭРБ относится пищевод Баррета, при котором резко (в 30-40 раз) повышается риск возникновения рака. ПБ обнаруживается при эндоскопии у 8-20% больных ГЭРБ. Распространенность ПБ в общей популяции значительно ниже и составляет 350 на 100 тыс. населения. По данным патологоанатомической статистики, на каждый известный случай приходится 20 нераспознанных. Причиной возникновения ПБ служит рефлюкс желудочного содержимого, и поэтому ПБ рассматривается как одно из проявлений ГЭРБ.
Механизм формирования ПБ можно представить следующим образом. При РЭ вначале повреждаются поверхностные слои эпителия, затем может образоваться дефект слизистой оболочки. Повреждение стимулирует локальную выработку факторов роста, что приводит к усилению пролиферации и метаплазии эпителия.
Клинически ПБ проявляется общими симптомами РЭ и его осложнениями. При эндоскопическом исследовании ПБ следует заподозрить в случае, когда ярко-красный метаплазированный эпителий в виде пальцевидных выпячиваний поднимается выше Z-линии (анатомический переход пищевода в кардию), вытесняя плоскоклеточный эпителий бледно-розового цвета, характерный для пищевода. Иногда в метаплазированной слизистой оболочке могут сохраняться множественные вкрапления плоскоклеточного эпителия - это так называемый «островковый тип» метаплазии. Слизистая оболочка вышележащих отделов может быть не изменена либо могут отмечаться явления эзофагита различной степени тяжести.
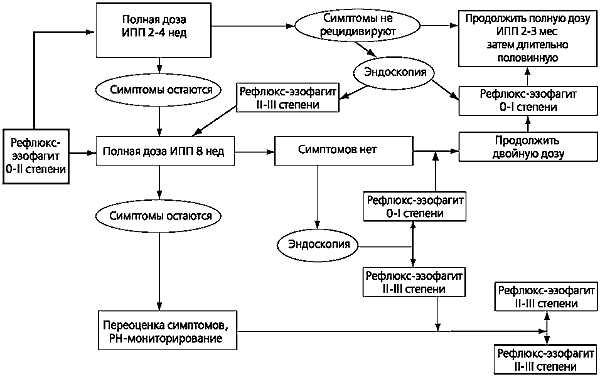
Рис. 1
Диагностика атипично протекающей ГЭРБ с легочными проявлениями
Эндоскопически выделяют два вида ПБ:
- короткий сегмент ПБ - распространенность метаплазии менее 3 см;
- длинный сегмент ПБ - распространенность метаплазии более 3 см.
При гистологическом исследовании ПБ на месте многослойного плоского эпителия находят элементы трех видов желез: одни сходны с фундальными, другие с кардиальными и третьи - с кишечными. Именно с кишечным эпителием в ПБ связывают высокий риск злокачественной трансформации. В настоящее время почти все исследователи считают, что о ПБ можно говорить только при наличии кишечного эпителия, маркером которого служат бокаловидные клетки (специализированный тип кишечного эпителия).
Оценка степени дисплазии метаплазированного эпителия при ПБ и ее дифференцирование со злокачественной трансформацией являются трудными задачами. Окончательное суждение о малигнизации в диагностически сложных случаях можно сделать при обнаружении мутации в туморсупрессивном гене р53.
Внепищеводные проявления ГЭРБ
Можно выделить следующие синдромы внепищеводных проявлений ГЭРБ.
1. Орофарингеальная симптоматика включает воспаление носоглотки и подъязычной миндалины, развитие эрозий эмали зубов, кариеса, периодонтита, фарингит, ощущение кома в горле.
2. Отоларингологическая симптоматика проявляется ларингитом, язвами, гранулемами и полипами голосовых складок, средним отитом, оталгиями и ринитом.
3. Бронхолегочная симптоматика характеризуется хроническим рецидивирующим бронхитом, развитием бронхоэкта-зов, аспирационной пневмонии, абсцессов легкого, пароксизмальным ночным апноэ и приступами пароксизмального кашля, а также бронхиальной астмой.
4. Боли в грудной клетке, связанные с заболеваниями сердца, проявляются рефлекторной стенокардией при рефлюксе содержимого желудка в пищевод.
5. Боли в грудной клетке, не связанные с заболеваниями сердца (non-cardiac chest pain), - частое осложнение ГЭРБ, требующее адекватной терапии на основе проведения тщательного дифференциального диагноза с кардиальной болью.
Установление связи бронхолегочных заболеваний с ГЭРБ имеет большую клиническую ценность, поскольку позволяет по-новому подойти к их лечению.
На рисунке 1 представлен алгоритм диагностики атипично протекающей ГЭРБ с легочными проявлениями, предложенный Американской ассоциацией гастроэнтерологов. Его основой является пробное лечение ИПП, и если при этом удается достигнуть положительного эффекта, то связь хронического респираторного заболевания с ГЭРБ считается доказанной. Дальнейшее лечение должно быть направлено на предупреждение заброса желудочного содержимого в пищевод и дальнейшего попадания рефлюксата в бронхолегочную систему.
Большие трудности могут возникнуть при дифференциальной диагностике загрудинных болей, связанных с заболеваниями сердца (стенокардия, кардиалгия) и другими заболеваниями, вызывающими загрудинные боли. Алгоритм дифференциальной диагностики представлен на рисунке 2. Помощь в распознавании загрудинных болей, связанных с ГЭРБ, может оказать суточное мониторирование рН пищевода (рис. 3).
Лечение
Цель лечения ГЭРБ - устранение жалоб, улучшение качества жизни, борьба с рефлюксом, лечение эзофагита, предотвращение или устранение осложнений. Лечение ГЭРБ чаще консервативное, чем хирургическое.
Консервативное лечение включает:
- рекомендации по соблюдению определенного образа жизни и диеты;
- медикаментозную терапию: антациды, антисекреторные препараты (блокаторы Н 2 -рецепторов и ингибиторы протонной помпы), прокинетики.
Разработаны следующие основные правила, которые постоянно должен соблюдать больной независимо от степени выраженности РЭ:
- после приема пищи избегать наклонов вперед и не ложиться;
- спать с приподнятым головным концом кровати;
- не носить тесную одежду и тугие пояса, корсеты, бандажи, приводящие к повышению внутрибрюшного давления;
- избегать обильных приемов пищи; не есть на ночь; ограничить потребление продуктов, вызывающих снижение давления НПС и обладающих раздражающим действием (жиры, алкоголь, кофе, шоколад, цитрусовые);
- отказаться от курения;
- снизить массу тела при ожирении;
- избегать приема лекарств, вызывающих рефлюкс (антихолинергические, спазмолитические, седативные препараты, транквилизаторы, ингибиторы кальциевых каналов, р-адреноблока-торы, теофиллин, простагландины, нитраты).
Антациды.
Цель антацидной терапии состоит в снижении кислотно-протеолитической агрессии желудочного сока. Повышая внутрижелудочный уровень рН, эти препараты устраняют патогенное действие соляной кислоты и пепсина в отношении слизистой оболочки пищевода. Арсенал современных антацидов достиг внушительных размеров. В настоящее время они выпускаются, как правило, в виде комплексных препаратов, основу которых составляют гидроокись алюминия, гидроокись или гидрокарбонат магния, неабсорбируемые в ЖКТ. Антациды назначаются 3 раза в день через 40-60 мин после еды, когда чаще всего возникает изжога, и на ночь. Рекомендуют придерживаться следующего правила: каждый приступ боли и изжоги следует купировать, поскольку эти симптомы указывают на прогрессирующее повреждение слизистой оболочки пищевода.
Антисекреторные препараты.
Антисекреторная терапия ГЭРБ проводится с целью уменьшения повреждающего действия кислого желудочного содержимого на слизистую оболочку пищевода при гастроэзофагеальном рефлюксе. Широкое применение при РЭ нашли блокаторы Н 2 -рецепторов (ранитидин, фамотидин). При использовании этих препаратов существенно снижается агрессивность забрасываемого желудочного содержимого, что способствует купированию воспалительного и эрозивно-язвен-ного процесса в слизистой оболочке пищевода. Ранитидин назначается однократно на ночь в суточной дозе 300 мг или по 150 мг 2 раза в день; фамотидин применяется однократно в дозе 40 мг или по 20 мг 2 раза в день.
Рис. 2.
Дифференциальная диагностика загрудинных болей

Рис. 3.
Эпизоды рецидивирующих загрудинных болей коррелируют с эпизодами рефлюса с рН<4 (В. Д. Пасечников, 2000).

В последние годы появились принципиально новые антисекреторные препараты - ингибиторы Н + ,К + -АТФазы (ИПП - омепразол, ланзопразол, рабепразол, эзомепразол). Ингибируя протонный насос, они обеспечивают выраженное и продолжительное подавление кислой желудочной секреции. ИПП отличаются особой эффективностью при пептичес-ком эрозивно-язвенном эзофагите, обеспечивая после 6-8 недель лечения заживление пораженных участков в 90-96% случаев.
В нашей стране наиболее широкое применения нашел омепразол. По антисекреторному эффекту этот препарат превосходит блокаторы Нг-рецепторов. Дозировка омепразола: 20 мг 2 раза в сутки или 40 мг в вечерние часы.
В последние годы в клинической практике широкое применение находят новые ИПП - рабепразол и эзомепразол (Нексиум).
Рабепразол быстрее других ИПП конвертируется в активную (сульфаниламидную) форму. Благодаря этому, уже в первый день приема рабепразола уменьшается или полностью исчезает такое клиническое проявление ГЭРБ, как изжога.
Значительный интерес представляет новый ИПП - эзомепразол (Нексиум), являющийся продуктом особой технологии. Как известно, стереоизомеры (вещества, молекулы которых имеют одинаковую последовательность химических связей атомов, но различное расположение этих атомов относительно друг друга в пространстве) могут отличаться по биологической активности. Пары оптических изомеров, являющихся зеркальными отображениями друг друга) обозначаются как R (от лат. rectus - прямой или rota dexterior - правое колесо, по часовой стрелке) и S (sinister - левый или против часовой стрелки).
Эзомепразол (Нексиум) - это S-изомер омепразола, первый и единственный в настоящее время ИПП, представляющий собой чистый оптический изомер. Известно, что S-изомеры других ИПП превосходят по фармакокинетическим параметрам их R-изомеры и соответственно рацемические смеси, которыми являются существующие сегодня лекарственные препараты этой группы (омепразол, ланзопразол, пантопразол, рабепразол). Создать стабильный S-изомер удалось пока только для омепразола. Исследования на здоровых добровольцах показали, что эзомепразол оптически устойчив в виде любой лекарственной формы - как для перорального, так и внутривенного применения .
Клиренс эзомепразола ниже, чем у омепразола и R-изомера. Следствием этого является более высокая биодоступность эзомепразола по сравнению с омепразолом. Иными словами, большая доля каждой дозы эзомепразола остается в кровотоке после метаболизма «первого прохождения». Таким образом, повышается количество препарата, осуществляющего ингибирование протонной помпы париетальной клетки желудка.
Антисекреторный эффект эзомепразола является дозозависимым, он возрастает в течение первых дней приема [ 11 ]. Действие эзомепразола наступает через 1 час после перорального приема в дозе 20 или 40 мг. При ежедневном приеме препарата в течение 5 дней в дозе 20 мг 1 раз сутки средняя максимальная концентрация кислоты после стимуляции пентагастрином снижается на 90% (измерение проводилось через 6-7 часов после приема последней дозы препарата). У пациентов с симптоматической ГЭРБ внутрижелудочный уровень рН при суточном мониторировании после 5-дневного приема эзомепразола в дозах 20 и 40 мг оставался выше 4 в течение в среднем 13 и 17 часов соответственно. Среди пациентов, принимавших эзомепразол по 20 мг в сутки, поддержание уровня рН выше 4 в течение 8, 12 и 16 часов достигалось в 76%, 54% и 24% случаев соответственно. Для 40 мг эзомепразола это соотношение составляло 97%, 92% и 56% соответственно (р <0,0001) .
Важным компонентом, обеспечивающим высокую стабильность антисекреторного действия эзомепразола, является его исключительно предсказуемый метаболизм. Эзомепразол обеспечивает в 2 раза большую стабильность такого показателя, как индивидуальная вариабельность подавления стимулированной пентагастрином желудочной секреции, чем омепразол в эквивалентной дозе .
Эффективность эзомепразола при ГЭРБ была изучена в нескольких рандомизированных двойных слепых многоцентровых исследованиях. В двух больших исследованиях, включавших более 4000 больных ГЭРБ, неинфицированных Н. pylori, эзомепразол в суточных дозах 20 или 40 мг был достоверно более эффективным в плане заживления эрозивного эзофагита, чем омепразол в дозе 20 мг . В обоих исследованиях эзомепразол значительно превосходил омепразол как после 4, так и 8 недель лечения.
Полное купирование изжоги (отсутствие в течение 7 последовательных дней) в группе из 1960 больных ГЭРБ также достигалось при лечении эзомепразолом в дозе 40 мг/сут у большего числа пациентов, чем при терапии омепразолом, как в 1 день приема препаратов (30% против 22%, р <0,001), так и к 28 дню (74% против 67%, р <0,001) . Аналогичные результаты были получены и в другом, большем по объему (п = 2425) исследовании (р <0,005) . В обоих исследованиях было показано преимущество эзомепразола над омепразолом (в эквивалентных дозах) как по среднему числу дней до наступления полного купирования изжоги, так и по суммарному проценту дней и ночей без изжоги в течение всего периода лечения. Еще в одном исследовании, включавшем 4736 больных эрозивным эзофагитом, эзомепразол в дозе 40 мг/сут достоверно превосходил омепразол в дозе 20 мг/сут по проценту ночей без изжоги (88,1%, доверительный интервал - 87,9-89,0; против 85,1%, доверительный интервал 84,2-85,9; р <0,0001) .Таким образом, наряду с известными клиническими показателями эффективности лечения ГЭРБ, указанные дополнительные критерии позволяют заключить, что эзомепразол объективно превосходит омепразол при лечении ГЭРБ. Столь высокая клиническая эффективность эзомепразола существенно повышает и его затратную эффективность. Так, например, среднее число дней до полного купирования изжоги при использовании эзомепразола в дозе 40 мг/сут составляло 5 дней, а оме-празола в дозе 20 мг/сут - 9 дней . При этом важно отметить, что омепразол в течение многих лет являлся золотым стандартом в лечении ГЭРБ, превосходя по клиническим критериям эффективности все другие ИПП, о чем свидетельствует анализ результатов более чем 150 сравнительных исследований .
Эзомепразол изучался и в качестве препарата для поддерживающей терапии ГЭРБ. В 2 двойных слепых, плацебо-контролируемых исследованиях, включавших более 300 больных ГЭРБ с зажившим эзофагитом, оценивалась эффективность трех дозировок эзомепразола (10, 20, и 40 мг/сут), назначавшихся в течение 6 месяцев .
Во всех изученных дозах эзомепразола существенно превосходили плацебо, но наилучшей с точки зрения соотношения доза/эффективность для поддерживающей терапии оказалась дозировка 20 мг/сут. Имеются опубликованные данные об эффективности поддерживающей дозы эзомепразола 40 мг/сут, назначавшейся 808 больным ГЭРБ: ремиссия через 6 и 12 месяцев сохранялась у 93% и 89,4% больных соответственно .
Уникальные свойства эзомепразола позволили применить совершенно новый подход к длительной терапии ГЭРБ - терапию по требованию, эффективность которой была изучена в двух 6-месячных слепых, плацебо-контролируемых исследованиях, включавших соответственно 721 и 342 больных ГЭРБ. Эзомепразол использовался в дозах 40 мг и 20 мг. В случае появления симптомов заболевания больным разрешалось использовать не более одной дозы (таблетки) в день, а если симптомы не купировались, то разрешалось принимать антациды. При подведении итогов оказалось, что в среднем больные принимали Эзомепразол (вне зависимости от дозы) 1 раз в 3 дня, при этом неадекватный контроль за симптомами (изжога) отметили лишь 9% больных, получавших 40 мг эзомепразола, 5% - 20 мг и 36% - плацебо (р <0,0001). Число больных, вынужденных дополнительно принимать антациды, оказалось в группе плацебо в 2 раза большим, чем в пациентов, получавших любую из дозировок эзомепразола .
Таким образом, клинические исследования убедительно свидетельствуют, что Эзомепразол является перспективным средством терапии ГЭРБ как при наиболее тяжелых ее формах (эрозивный эзофагит), так и при неэрозивной рефлюксной болезни.
Прокинетики.
Представители этой группы лекарственных веществ обладают антирефлюксным действием, а также усиливают высвобождение ацетилхолина в желудочно-кишечном тракте, стимулируя моторику желудка, тонкой кишки и пищевода. Они повышают тонус НПС, ускоряют эвакуацию из желудка, оказывают положительное влияние на пищеводный клиренс и ослабляют гастроэзофагеальный рефлюкс.
В качестве прокинетика при РЭ обычно используется домперидон, который является антагонистом периферических дофаминовых рецепторов. Домперидон назначается по 10 мг (1 таблетка) 3 раза в день за 15-20 мин до еды.
При РЭ, обусловленном забросами в пищевод дуоденального содержимого (в первую очередь, желчных кислот), что обычно наблюдается при желчнокаменной болезни, хороший эффект достигается при приеме нетоксической урсоде-оксихолевой желчной кислоты в дозе 5 мг/кг в сутки в течение 6-8 мес.
Выбор тактики лечения.
При выборе лечения ГЭРБ в стадии эрозивно-язвен-ного РЭ следует помнить, что в этих случаях терапия является непростой задачей. Заживление дефекта слизистой оболочки в среднем происходит:
- за 3-4 недели при язве двенадцатиперстной кишки;
- за 4-6 недель при язве желудка;
- за 8-12 недель при эрозивно-язвенных поражениях пищевода.
В настоящее время разработана схема поэтапного лечения в зависимости от степени выраженности РЭ. Согласно этой схеме, уже при РЭ 0 и I степени рекомендуется начинать лечение с полной дозы ИПП, хотя допускается и применение Н 2 -блокаторов в сочетании с прокинетиками (рис. 4).
Схема лечения больных с тяжелым РЭ (II-III ст.) представлена нарисунке 5. Особенность этой схемы состоит в более продолжительных циклах лечения и назначении (при необходимости) высоких доз ИПП. При отсутствии эффекта от консервативного лечения у больных этой категории нередко приходится ставить вопрос о проведении антирефлюксного хирургического вмешательства. Целесообразность оперативного лечения должна обсуждаться и при осложнениях РЭ, не поддающихся медикаментозной терапии.
Хирургическое лечение.
Целью операций, направленных на устранение рефлюкса, является восстановление нормальной функции кардии.
Показания к оперативному лечению: 1) безуспешность консервативного лечения; 2) осложнения ГЭРБ (стриктуры, повторные кровотечения); 3) частые аспирационные пневмонии; 4) ПБ (из-за опасности малигнизации). Особенно часто показания к операции возникают при сочетании ГЭРБ с грыжей пищеводного отверстия диафрагмы.
Основным типом операции при рефлюкс-эзофагите является фундопликация по Ниссену. В настоящее время разрабатываются и внедряются методы фундопликации, проводимой через лапароскоп. Преимущества лапароскопической фундопликации состоят в существенно более низких показателях послеоперационной летальности и быстрой реабилитации больных.
В настоящее время при ПБ для воздействия на очаги неполной кишечной метаплазиии и тяжелой дисплазии эпителия используют следующие эндоскопические методики:
- лазерная деструкция, коагуляция аргоновой плазмой;
- мультиполярная электрокоагуляция;
- фотодинамическая деструкция (за 48-72 ч до процедуры вводят фото-сенсибилизирующие препараты, затем воздействуют лазером);
- эндоскопическая локальная резекция слизистой оболочки пищевода.
Все перечисленные методы воздействия на очаги метаплазии используются на фоне применения ИПП, подавляющих секрецию, и прокинетиков, уменьшающих гастроэзофагеальный рефлюкс.
Профилактика и диспансеризация
В связи с широким распространением ГЭРБ, приводящей к снижению качества жизни, и опасностью осложнений при тяжелых формах РЭ профилактика этого заболевания является весьма актуальной задачей.
Цель первичной профилактики ГЭРБ состоит в предупреждении развития заболевания. Первичная профилактика включает соблюдение следующих рекомендаций:
- соблюдение здорового образа жизни (отказ от курения и приема крепких алкогольных напитков);
- рациональное питание (избегать обильных приемов пищи, не есть на ночь, ограничить потребление очень острой и горячей пищи;
- снижение массы тела при ожирении;
- только по строгим показаниям осуществлять прием лекарств, вызывающих рефлюкс (антихолинергические, спазмолитические, седативные препараты, транквилизаторы, ингибиторы каль циевых каналов, b-адреноблокаторы, простагландины, нитраты) и повреждающих слизистую оболочку (нестероидные противовоспалительные препараты).
Рис. 4.
Выбор лечения больных с эндоскопически негативным или с легкими (0-1) степенями рефлюкс-эзофагита

Рис. 5.
Выбор лечения больных с тяжелыми (II- III) степеням рефлюкс-эзофагита
Цель вторичной профилактики ГЭРБ -снижение частоты рецидивов и предотвращение прогрессирования заболевания. Обязательным компонентом вторичной профилактики является соблюдение вышеизложенных рекомендаций по первичной профилактике. Вторичная медикаментозная профилактика во многом зависит от степени выраженности РЭ.
«Терапия по требованию» используется для профилактики обострений при отсутствии эзофагита или легком эзофагите (РЭ 0-1 степени). Каждый приступ боли и изжоги следует купировать, поскольку это сигнал патологического за-кисления пищевода, способствующего прогрессирующему повреждению его слизистой оболочки. Тяжелый эзофагит (особенно РЭ III-IV степени) требует длительной, порой постоянной поддерживающей терапии ИПП или блокаторами Н 2 -рецепторов в сочетании с прокинетиками.
Критериями успешной вторичной профилактики принято считать уменьшение числа обострений заболевания, отсутствие прогрессирования, снижение степени тяжести РЭ и предупреждение развития осложнений.
Больные ГЭРБ при наличии эндоскопических признаков РЭ нуждаются в диспансерном наблюдении с эндоскопическим контролем не реже одного раза в 2-3 года.
В особую группу следует выделять больных, у которых диагностирован ПБ. Эндоскопический контроль с проведением прицельной биопсии слизистой оболочки пищевода из зоны визуально измененного эпителия желательно проводить ежегодно (но не реже 1 раза в год), если при предыдущем исследовании отсутствовала дисплазия. При обнаружении последней эндоскопический контроль следует проводить чаще, чтобы не пропустить момента малигнизации. Наличие при ПБ дисплазии низкой степени требует эндоскопии с биопсией каждые 6 месяцев, а тяжелой дисплазии - через 3 мес. У больных с подтвержденной тяжелой дисплазией следует ставить вопрос об оперативном лечении.
ЛИТЕРАТУРА
1. Dean ВВ, CrawleyJA, SchmittCM, Wong], Of man 11. The burden of illness of gastro-oesophageal reflux disease: impact on work productivity. Aliment Pharmacol Ther2003 May 15;17:1309-17.
2. DentJ, Jones R, Kahrilas P, Talley N1. Management of gastro-oesophageal reflux disease in general practice. BMJ 2001;322:344-7.
3. GalmicheJP, LetessierE, Scarpignato C. Treatment of gastro-oesophageal reflux disease in adults. BMJ 199S;316:1720-3.
4. Kahrilas PI. Gastroesophageal reflux desease. JAMA 1996:276:933-3.
5. Salvatore S, Vandenplas Y. Gastro-oesophageal reflux disease and motility disorders. Best Pract Res Clin Gastroenterol 2003:17:163-79.
6. Stanghellini V. Management of gastroesophageal reflux disease. Drugs Today (Bare) 2003;39(suppl. A):15-20.
7. Arimori K, Yasuda K, Katsuki H, Nakano M. Pharmacokinetic differences between lansoprazole enantiomers in rats. J Pharm Pharmacol 1998:50:1241-5.
8. Tanaka M, Ohkubo T, Otani K, et al. Stereoselective pharmacokinetics of pantopra-zole, a proton pump inhibitor, in extensive and poor metabolizers of S-mephenytoin. Clin Pharmacol Ther 2001:69:108-13.
9. Abelo A, Andersson ТВ, Bredberg U, et al. Stereoselective metabolism by human liver CYP enzymes of a substituted benzimidazole. Drug Metab Dispos 2000:28:58-64.
10. Hassan-Alin M, Andersson T, Bredberg E, Rohss K. Pharmacokinetics of esomeprazole after oral
and intravenous administration of single and repeated doses to healthy subjects. Eur 1 Clin Pharmacol 2000:56:665-70.
11. Andersson T, Bredberg E, Hassan-Alin M. Pharmacokinetics and pharmacodynamics of esomeprazole, the S-isomer of omeprazole. Aliment Pharmacol Ther 2001:15:1563-9.
12. Lind T, Rydberg L, Kyleback A, et al. Esomeprazole provides improved acid control vs. omeprazole in patients with symptoms ofgastro-oesopageal reflux disease. Aliment Pharmacol Ther 2000:14:861-7.
13. Andersson T, Rohss K, Hassan-Alin M. Pharmacokinetics (PK) and dose-response relationship of esomeprazole (E). Gastroenterology 2000:118(suppl. 2):A1210.
14. Kahrilas PI, Falk GW, Johnson DA, et al. Esomeprazole improves healing and symptom resolution as compared with omeprazole in reflux oesophagitis patients: a randomized controlled trial. The Esomeprazole Study Investigators. Aliment Pharmacol Ther 2000:14:1249-58.
15. RichterJE, Kahrilas PJ, JohansonJ, et al. Efficacy and safety of esomeprazole compared with omeprazole in GERD patients with erosive esophagitis: a randomized controlled trial. Am 1 Gastroenterol 2001:96:656-65.
16. Vakil NB, Katz PO, Hwang C, et al. Nocturnal heartburn is rare in patients with erosive esophagitis treated with esomeprazole . Gastroenterology 2001:120:abstract 2250.
17. Kromer W, Horbach S, Luhmann R. Relative efficacies of gastric proton pump inhibitors: their
clinical and pharmacological basis. Pharmacology 1999: 59:57-77.
18. Johnson DA, Benjamin SB, Vakil NB, et al. Esomeprazole once daily for 6 months is effective therapy for maintaining healed erosive esophagitis and for controlling gastroesophageal reflux disease symptoms: a randomized, double-blind, placebo-controlled study of efficacy and safety. Am 1 Gastroenterol 2001:96:27-34.
19. Vakil NB, Shaker R, Johnson DA, et al. The new proton pump inhibitor esomeprazole is effective as a maintenance therapy in GERD patients with healed erosive oesophagitis: a 6-month, randomized, double-blind, placebo-controlled study of efficacy and safety. Aliment Pharmacol Ther 2001:15:927-35.
20. Ma ton P N, Vakil N B, Levine JG, et al. Sa fety fnd efficacy of long term esomeprasole therapy in patients with healed erosive oesophagitis. Drug Saf 2001:24:625-35.
21. Talley N1, Venables TL, Green JBR. Esomeprazole 40mg and 20mg is efficacious in the lomg-tenn management of patients with endoscopy-nega-tive GERD: a placebo-controlled trial of on-demand therapy for 6 months. Gastroenterology 2000:118:A658.
22. Talley N1, Lauritsen K, Tunturi-Hihnala H, et al. Esomeprazole 20 mg maintains symptom control in endoscopy-negative gastro-oesophageal reflux disease: a controlled trial of "on-demand" therapy for 6 months. Aliment Pharmacol Ther 2001:15:347-54.
Гастроэзофагеальный рефлюкс – симптомокомплекс, характеризующий передвижение содержимого желудка в обратном направлении (в пищевод). В некоторых случаях это может быть нормальным явлением, в других – провоцировать серьезные патологии.
Гастроэзофагеальный рефлюкс – причины
Заброс содержимого из желудка, происходящий в единичных случаях непосредственно после употребления пищи, не причиняющий человеку дискомфорта и не вызывающий других нарушений, считается вариантом нормы. Если же это происходит часто, в том числе ночью, сопровождается очевидными симптомами, речь идет об отклонении, приводящем к развитию гастроэзофагеальной рефлюксной болезни.
Рассматривая причины гастроэзофагеального рефлюкса, следует понять механизм заброса содержимого в неправильном направлении. Большую роль в предотвращении данного явления играет нижний пищеводный сфинктер – мышца, почти все время пребывающая в сомкнутом состоянии и раскрывающаяся в двух случаях – при перемещении пищевого кома в желудок и при выходе наружу проглоченного воздуха.
Спонтанное расслабление нижнего сфинктера пищевода может быть связано как с его функциональными нарушениями, так и со снижением мышечного тонуса. Последнее очень часто провоцируется такими факторами:
- употребление кофеинсодержащих напитков;
- употребление горячих блюд и напитков;
- прием некоторых лекарств (спазмолитики, анальгетики, нитраты и пр.);
- курение;
- употребление алкоголя;
- интенсивные физические нагрузки;
- изменение гормонального фона.

Помимо этого, предпосылкой для обратного заброса иногда является повышенное внутрибрюшное давление, наблюдаемое при излишней массе тела, асците, запорах, метеоризме. Внутрижелудочное давление провоцируется употреблением газированных напитков, жареных блюд, острыми специями. Также условия для рефлюкса имеются при грыже пищеводного отверстия диафрагмы, язвенной болезни, бронхиальной астме.
В патологичности гастроэзофагеального рефлюкса имеет значение не только непосредственно заброс, но и возможность пищевода освобождаться от попадающего раздражителя. В норме при попадании кислого желудочного содержимого восстановление рН и возврат обратно в желудок посредством усиления перистальтики пищевода и выделения слюны происходит быстро (эта способность называется пищеводным клиренсом).
Гастроэзофагеальный рефлюкс – симптомы
В типичной клинической картине следующие признаки гастроэзофагеального рефлюкса являются определяющими:
- отрыжка;
- ощущение комка в горле;
- дискомфорт при проглатывании пищи;
- рвота;
- тошнота;
- загрудинная боль, напоминающая приступ стенокардии.
Во многих случаях, особенно при «высоких» рефлюксах отмечается ряд так называемых внеэзофагеальных симптомов:
- кашель;
- одышка;
- воспаление слизистой гортани, носоглотки, бронхов;
- осиплость голоса;
- кариес, .
Патологические проявления усиливаются в ночное время, после приема пищи, при физических нагрузках. При наличии характерных симптомов гастроэзофагеальная рефлюксная болезнь может протекать в одной из двух форм:
- с воспалительными изменениями пищеводных стенок, выявляемыми эндоскопическим методом (с эзофагитом);
- без воспаления пищевода, устанавливаемого посредством эндоскопа (без эзофагита).
Гастроэзофагеальный рефлюкс без эзофагита
В данном случае гастроэзофагельная рефлюксная болезнь именуется неэрозивной. При этом слизистая ткань пищевода является защищенной от поступления в орган содержимого, которое не свойственно ему, т.е. клиренс находится в норме. Кроме того, в обеспечении регенерации эпителия играет роль нормальная микроциркуляция в сосудах и лимфатических капиллярах. Эпизоды рефлюкса с проявлениями повторяются не очень часто, однако это может являться предшествующей стадией эрозивного процесса.
Гастроэзофагеальный рефлюкс с эзофагитом
Если гастроэзофагеальный рефлюкс сопряжен с высокой частотой затекания желудочного содержимого, повышается риск патологических изменений слизистой пищеводного тракта. Способствует этому и повышенная агрессивность рефлюката, связанная с прочими заболеваниями (например, при повышенной кислотности, наличии желчных кислот). Клиническая картина, в основном, складывается из желудочно-кишечных проявлений. При этом нередко сопровождает гастроэзофагеальный рефлюкс кашель – сухой, возникающий зачастую днем, усиливающийся при изменениях положения тела.

Гастроэзофагеальный рефлюкс – степени
Патологический гастроэзофагеальный рефлюкс – это следствие ослабления защитных механизмов пищевода и агрессивности повреждающих факторов. В зависимости от масштаба повреждений патологию классифицируют на степени. Приведем одну из применяемых классификаций:
- 0 степень – клинические проявления отсутствуют:
- I степень – наличие отдельных очагов эрозии на фоне гиперемированной ткани, занимающих не больше 10 % дистального отдела пищевода;
- II степень – имеются сливающиеся участки эрозии, на которые приходится до 50 % поверхности дистального отдела;
- III степень – множественные язвенные повреждения, занимающие поверхность дистального отдела полностью;
- IV степень – развитие осложнений: глубокие язвы, сужение пищевода, пищевод Баррета и пр.
Гастроэзофагеальный рефлюкс - диагностика
Предварительный диагноз нередко ставится на основании жалоб и анамнеза. Для установления того, к какой форме относится гастроэзофагеальный рефлюкс, визуальная диагностика имеет ведущее значение. Проведение эзофагогастродуоденоскопии дает широкую картину поражения и сопутствующих отклонений. При необходимости проводится биопсия. Кроме этого, могут потребоваться такие методы:
- рентген-диагностика с барием;
- суточный мониторинг рН пищевода;
- эзофаготонокимография;
- билиметрия;
- сцинтиграфия.
Как лечить гастроэзофагеальный рефлюкс?
Диагностируемый патологический гастроэзофагеальный рефлюкс лечение должен иметь комплексное, при этом приоритетную роль играет медикаментозная терапия. Важным является соблюдение диеты и выполнение следующих рекомендаций:
- снижение массы тела;
- ограничение подъема грузов (не более 10 кг);
- избегание наклонов и напряжения пресса;
- отказ от стесняющей одежды;
- сон на высокой подушке;
- отказ от вредных привычек.

Гастроэзофагеальный рефлюкс – лечение, препараты
Во избежание осложнений гастроэзофагеальный рефлюкс с эзофагитом лечение обязательно должен иметь медикаментозное. В зависимости от тяжести патологии, назначаются препараты, относящиеся к таким группам:
- – (Фосфалюгель, Маалокс);
- альгинаты (Гевискон);
- прокинетики (Мотилиум);
- ингибиторы протонной помпы (Омез, Ланзоптол);
- блокаторы H2-рецепторов гистамина (Ранисан, Фамотидин).
Некоторые из приведенных препаратов принимаются эпизодически для купирования симптомов, другие требуют курсового приема до стойкого устранения проявлений. При рефлюксе без эзофагита показано только назначение антацидов и альгинатов. При тяжелых степенях болезни может потребоваться хирургическое вмешательство (например, фундопликация по Ниссену).
Гастроэзофагеальный рефлюкс – лечение народными средствами
В стадии ремиссии, когда гастроэзофагеальный рефлюкс не имеет выраженных проявлений, допустимо использование нетрадиционных методов в профилактических целях. Пациентам, у которых диагностирован гастроэзофагеальный рефлюкс, народное лечение предлагает, в основном, использование фитотерапевтических средств обволакивающего и противовоспалительного действия. Приведем один из рецептов.
Травяной настой
Нам хотелось бы предварить обсуждение терапевтических возможностей при гастроэзофагеальной рефлюксной болезни (ГЭРБ) краткой информацией по механизмам развития и диагностики этой патологии. Возможности хирургического лечения ГЭРБ в данной статье затрагиваться не будут.
Определение
Итак, А.С. Трухманов определяет ГЭРБ как возникновение характерных симптомов и (или) воспалительное поражение дистальных участков пищевода вследствие повторяющегося заброса в пищевод желудочного содержимого .
Согласно определению Международной рабочей группы термин "гастро-эзофагиальная рефлюксная болезнь" должен применяться ко всем индивидуумам подверженным риску соматических осложнений гастро-эзофагельного рефлюкса, или испытывающим значительное ухудшение связанного со здоровьем благосостояния (качества жизни), в результате симптомов рефлюкса, после адекватного убеждения в доброкачественной природе симптомов .
Термин "эндоскопически негативная рефлюксная болезнь" должен быть применяться у лиц соответствующих определению гастро-эзофагиальной рефлюксной болезни, но у которых отсутствует как пищевод Барретта, так и видимые дефекты слизистой (эрозии или язвы) при эндоскопическом исследовании .
Механизмы развития
Не останавливаясь подробно на патогенетических механизмах развития данного заболевания, скажем только, что в его основе лежит воздействие кислоты и пепсина на слизистую пищевода вследствие сочетания (в различных пропорциях) патологического рефлюкса желудочного содержимого в пищевод с нарушением его клиренса. Патологический рефлюкс содержимого, в свою очередь обусловлен нарушением функции нижнего пищеводного сфинктера (либо в результате снижение его тонуса или увеличения частоты спонтанных расслаблении, либо вследствие его анатомического дефекта, например при грыже ПОД). В основе нарушения клиренса пищевода могут лежать снижение выработки слюны или нарушение перистальтики пищевода. В результате всего вышесказанного происходит нарушение баланса между факторами агрессии и факторами защиты, что и приводит, но не обязательно, к возникновению рефлюск-эзофагита.
Эпидемиология
По данным С.И. Пимaнова эпизодически симптомы ГЭРБ наблюдаются у половины взрослого населения, а эндоскопическая картина эзофагита наблюдается у 2-10 % обследованных людей . Необходимо помнить о том, что ГЭРБ далеко не всегда сопровождается эзофагитом. До 50 - 70 % пациентов с изжогой на момент обращения за медицинской помощью имеют эндоскопически негативную ГЭРБ . Существующее у ряда практических врачей отношение к эндоскопически негативной ГЭРБ как к наиболее легкой степени этого заболевания не требующей интенсивной медикаментозной терапии в корне неверно. Ряд исследований продемонстрировал, что качество жизни у пациентов с эндоскопически позитивной и негативной ГЭРБ нарушается в практически одинаковой степени . Проведенные исследования показали, что эндоскопически негативная ГЭРБ весьма редко переходит в рефлюкс эзофагит, а тот в свою очередь редко прогрессирует в более тяжелые формы в течение времени .
Диагностика
Поскольку диагностика ГЭРБ широко описана во многих руководствах остановимся только на некоторых ее моментах. Основным симптомом ГЭРБ наблюдающимся у по крайней мере 75 % пациентов является изжога . Так же может иметь место боль или чувство жжения грудиной, отрыжка и т.д. Чаще всего симптомы ГЭРБ возникают после еды.
Диагностика эрозивного эзофагита проводиться на основе эндоскопического обследования. Рентгенография с барием имеет достаточно высокую чувствительность при тяжелом (98,7 %) и средней тяжести (81,6 %) эзофагитах, но малочувствительная (24, 6 %) при его легкой степени . Эндоскопия с биопсией является единственным надежным методом диагностики пищевода Барретта. Степени тяжести эрозивного рефлюкс эзофагита на эндоскопической картины делятся на 4 степени A, B, C и D (по классификации Los Angeles).
Мониторирование рН является чувствительным и специфичным диагностическим тестом и особенно важно для выявления эндоскопически негативной ГЭРБ. Более 50 эпизодов снижения рН ниже 4 рассматривается в качестве диагностического критерия ГЭРБ . У ряда больных происходит менее значительное снижение рН пищевода, но при совпадении большинства эпизодов такого снижения с моментами возникновением симптомов позволяет говорить о "гиперчувствительном пищеводе".
Среди провокационных тестов определенную роль играет тест Бернштейна (возникновение типичных симптомов после введения в пищевод слабого раствора соляной кислоты и их исчезновение после введения физиологического раствора). Определение давления нижнего пищеводного сфинктера полезно при решении вопроса об оперативном лечении.
Лечение
Прежде чем перейти к рассмотрению отдельных аспектов лечения ГЭРБ необходимо подчеркнуть факт, что основной его задачей является скорейшее избавление пациентов от беспокоящих его симптомов. Исчезновение симптоматики как правило хорошо коррелирует с заживлением дефектов слизистой при эрозивной эзофагите .
Изменение стиля жизни.
Хотя по данным рабочей группы по ГЭРБ факторы стиля жизни и не играют определяющей роли в развитии ГЭРБ , рекомендации направлены на устранение факторов способствующих рефлюксу или ухудшающих клиренс пищевода должны быть даны.
Диета. Необходимо прекратить прием индуцирующих рефлюкс продуктов (жирной пищи, шоколада и чрезмерного количества алкоголя, лука и чеснока, кофе, газированные напитки, особенно различные виды кол) и препаратов с низким рН (апельсиновый и ананасный соки, красное вино). Однако попытка резко ограничить диету пациента (особенно молодого возраста) редко возможно на практике, ваши рекомендации просто не будут выполняться. Разумнее выявить какие продукты вызывают появление или обострение симптоматики у данного конкретного пациента и попытаться отказаться хотя бы от них. Больной должен быть информирован, что необходимо избегать переедания. После еды желательно не принимать горизонтальное положение и не работать в наклон. Последний прием пище должен быть за 3 часа до сна.
Контроль веса. Похудание не всегда ведет к разрешению симптоматики, но снижение массы тела может снизить риск развития грыжи пищеводного отверстия диафрагмы. Однако дать совет - похудеть, гораздо легче, чем его выполнить. Полные люди иногда стараются скрыть отсутствие талии путем чрезмерного затягивания поясного ремня, что приводит к повышению внутрибрюшного давления и развитию рефлюксу (как и ношении слишком обтягивающей одежды).
Курение - фактор способствующий ГЭРБ в результате, как расслабления сфинктера, так и уменьшения саливации и соответственно должно быть прекращено . Хотя по данным ряда исследователей прекращение курения имеет минимальный положительный эффект при ГЭРБ .
Подъем головного конца кровати важен для пациентов с ночными или ларенгеальными симптомами (которые составляют небольшую часть пациентов с ГЭРБ), его необходимость в других случаях сомнительна.
Ряд лекарственных препаратов как спазмолитики, бета блокаторы, снотворные и седативные средства нитраты и антагонисты кальция могут способствовать развитию рефлюкса.
Антациды.
Обсуждая применение антацидов, которых в наше время существует великое множество (альмагель, фосфалюгель, маалокс, рутацид и т.д.), хотелось бы подчеркнуть, что по нашему мнению антациды самостоятельной роли в лечении ГЭРБ не играю и могут применяться только в качестве средства кратковременного контроля симптомов. В основе низкой эффективности антацидов лежит кратковременность контроля рН достигаемого их применением. Данные многих авторов подтверждают минимальный эффект антацидов (даже в сочетании с изменением стиля жизни) при рефлюкс-эзофагите, хотя он и превосходит эффект плацебо . Мы предлагаем пациентам (получающим лечение по поводу ГЭРБ) применять антациды в качестве метода быстрого контроля симптомов возникших, как правило, после нарушения диеты или физических упражнений и лицам с редкими (не более 4х в месяц) эпизодами изжоги без эндоскопических признаков эзофагита.
Антисекреторные препараты.
Наиболее эффективным способом лечения ГЭРБ является снижение кислотопродукции в желудке с помощью Н2 блокаторов или ингибиторов протонной помпы. Целью такой терапии является повышение рН желудочного сока до 4 и в период наибольшей вероятности возникновения рефлюкса т.е. не профилактика рефлюкса как такового, а элиминации патологического воздействия компонентов желудочного сока на пищевод. Н2 блокаторы. До появления ингибиторов протонной помпы Н2 блокаторы являлись препаратом выбора в лечении ГЭРБ. В практике в настоящее время используются 4 блокатора Н2 гистаминовых рецепторов (циметидин, ранитидин, фамотидин и низатидин). Механизм действия препаратов заключается в блокировании желудочной секреции стимулируемой гистамином. Однако два других пути стимуляции - ацетилхолиновый и гастриновый остаются открытыми. Именно с этим фактом и связанна меньшая чем у ингибиторов протонной помпы (PPI) степень подавления секреции и постепенное уменьшение степени ингибирования желудочной секреции при длительном использовании Н2 блокаторов, когда стимуляция кислотопродукции начинает все в большей степени осуществляться через другие медиаторы (преимущественно гастрин).
Циметидин (Н2 блокатор первого поколения). Применяют по 200 мг 3-4 раза в день и 400 мг на ночь. Максимальная суточная доза 12 грамм.
Ранитидин (второе поколение) применяется в дозировке 150 мг 2 раза в сутки, которая может, при необходимости достигать 300 мг 2 раза в сутки (максимальная доза 9 грамм в сутки). При ночных симптомах - 150-300 мг на ночь. Поддерживающая терапия - 150 мг на ночь.
Фамотидин (третье поколение) используется в дозе 20 мг два раза в день, максимальная суточная доза 480 мг. При ночных симптомах 20-40 мг на ночь, поддерживающая терапия 20 мг на ночь.
Низатидит (четвертое поколение) принимается по 150 мг два раза в день или 300 мг перед сном.
В связи с очень широким спектром побочных эффектов (от андрогенного действия до блокады дыхательных ферментов) и неудобной дозировки циметидин в настоящее время в практике не используется. Из всех других Н2 блокаторов мы предпочитаем фамотидин (как препарат с наименее часто встречающимися побочными эффектами). Необходимо помнить, что все H2 блокаторы отменяются постепенно, что бы предупредить синдром "отдачи" - резкого повышения кислотности после прекращения лечения.
На основании 33 рандомизированных исследований (включавших 3000 человек) были получены следующие данные: применение плацебо приводило к облегчению симптоматики ГЭРБ у 27 % пациентов, Н2 блокаторов у 60 % и PPI у 83 % . Эзофагит купировался в 24 %, 50 % и 78 % случаев соответственно. Эти цифры позволяют сделать вывод об эффективности Н2 блокаторов в лечении ГЭРБ, которая однако, значительно уступает таковой у PPI. Н2 блокаторы сохраняют определенную роль в терапии ГЭРБ. Они эффективны в качестве терапии рефлюкса возникающего в ночное время , даже в случае продолжающегося приема PPI и как терапия "по требованию".
Блокаторы протонной помпы.
Действие их основано на блокировании АТФ-азы притонного насоса (за счет образования необратимой связи с цистиновым остатком энзима). Необходимо помнить, что PPI блокирует только активный в настоящий период протонный насос. Препараты этой группы всасываются в виде неактивных соединений переходя в активное действующее вещество непосредственно в канальцевых системах секреторных клеток. Все PPI, кроме эзомепразола, имеют короткий период полувыведения (30 - 120 минут). Разрушение PPI происходит в печени, причем существует два пути их разрушения - быстрый и медленный. Процесс разрушения стереозависем. Правовращающий изомер распадается по быстрому пути, левовращающийся по медленному. Все PPI, опять же кроме эзомепразола (только левовращающий изомер), представлены право и левовращающими изомерами. Этот факт и объясняет более длительное сохранение эзомепразолом минимальной терапевтической концентрации по сравнению с другими PPI.
PPI назначаются до еды, (обычно за 30 минут до завтрака, при однократном приеме), что бы действие наступило в момент наличие максимального количества активных протоновых помп - 70 - 80 % от их общего количества. Следующая доза PPI снова блокирует 70-80 % рецепторов (оставшихся и регенерировавших), таким образом пик антисекреторного эффекта наступает на 2-3 сутки (несколько быстрее при использовании эзомепразола). PPI практически не эффективны как терапия по требованию (возникновение симптомов - изжоги, указывает на уже произошедший выброс кислоты, с последующим, как правило, снижением числа активных помп и, следовательно, отсутствием мишени для действия PPI).
При анализе сравнительной эффективности различных PPI можно сделать вывод об отсутствии существенных преимуществ между омепразолом, рабепразолом, лансопразолом и пантопразолом. Эффективность эзомепразола (нексиума) несколько выше. При сравнении длительности сохранения внутрижелудочной рН > 4 с использованием различных PPI были получены данные о лучшем контроле желудочной секреции при использовании нексиума (рис. 1).
Хотя следует заметить, что при использовании 40 мг омепразола разница не столь заметна. Преимущества нексиума более выражены при тяжелых формах эзофагита (степень D) . Омепразол используется в дозе 20 - 40 мг в сутки (либо однократный прием утром, либо два раза в сутки). В тяжелых случаях доза может достигать 60 мг в сутки. Лансопразол применяется по 30 мг/сут, пантопразол по 40 мг/сут, рабепразол по 20 мг/сут и нексиум по 40 мг/сут. Отмена препарата так же должна быть постепенной.
Прокинетические препараты.
Прокинитические препараты (домперидон, метоклопрамид и цизаприд) могут усиливать давление нижнего пищеводного сфинктера, улучшать пищеводный клиренс и ускорять опорожнение желудка. Цизаприд доступен только к ограниченному применению в США из-за опасений связанных с сердечными аритмиями (см. ниже). Метоклопамид в 20-50% случаев вызывает слабость, беспокойство, тремор, паркинсонизм или позднюю дискинезию. Применяется по 10 мг 3-4 раза в сутки. Максимальная разовая доза 20 мг, суточная 60 мг.
Цисаприд. Хотя цизаприд обычно считался практически безопасным его недавнее широкое использование в США было связанно с возникновением сердечных аритмий. Наиболее часто они развивались при приеме цизаприда в комбинации с препаратами ингибирующими цитохром Р-450 и повышают уровень цизаприда. В результате этого производитель частично ограничил использование этого препарата в США. Проведенные исследования по сравнению эффективности цисаприда 910 мг четыре раза в день) с антогонистами Н2 рецепторов (ранитидин 150 мг два раза вдень) и циметидин (400 мг 4 раза в день) продемонстрировали их превосходство над плацебо и сходную эффективность в купировании симптомов ГЭРБ и излечении эзофагита . Комбинация Н2 блокаторов с цисапридом дает лучший эффект чем каждый из препаратов в отдельности, но уступает омепразолу .
Домперидон (мотилиум) по механизму действия сходен с метоклопрамидом, но не проникает через гематоэнцефалический барьер и следовательно, не вызывает центральных побочных действий, но повышает уровень пролактина в крови. Применяется по 10 мг 3-4 раза в день. Не один из препаратов не дал хорошего терапевтического эффекта при тяжелых степенях эзофагита.
Роль НР инфекции.
В настоящее время роль Нр инфекции при ГЭРБ остается дискутабельной. Хотя согласно Маастрикским соглашениям ГЭРБ и является показанием к проведению эрадикационной терапии, далеко не все авторы с этим согласны. Ряд исследований показало, что эрадикация Нр не приводит к излечению рефлюкс эзофагита, как и не имеет профилактической роли в плане его рецидива . Тот факт, что инфекция Нр может вызывать как усиление, так и снижение секреторной функции желудка делает ее роль в развитии ГЭРБ еще более дискутабельной. Данные некоторых авторов даже указывают на протективную роль Нр инфекции при ГЭРБ , за счет ощелачивающего действия, а в дальнейшем развитии атрофии слизистой.
Практически единственным фактором, оправдывающим эрадикационную терапию при ГЭРБ, является то, что хроническое применение PPI, на фоне существующей Нр инфекции, способствует развитию атрофического гастрита и метаплазии . По данным Kuipers EJ сравнивающего вероятность развития атрофического гастрита в группах пациентов с ГЭРБ и Нр инфекцией получавших омепразол или подвергшихся фундопликации, он развивался у 31 % и 5 % больных соответственно. Хотя другое исследование такой закономерности не обнаружило . В свою очередь эрадикационная терапия не вызывает обострения или утяжеления ГЭРБ .
В нашей практике мы тестируем на наличие Нр и проводим эрадикацию пациентам с ГЭРБ только при условии наличии у них сопутствующего заболевания верхнего отдела ЖКТ связь которого с Нр инфекцией установлена (например язвенная болезнь) или при планировании хронического (более года) постоянного приема ингибиторов протонной помпы.
Новые направления фармакотерапии.
По данным Ciccaglione et al препарат снижающий число спонтанных расслаблении нижнего пищеводного сфинктера баклофен в дозировки 10 мг 3 раза в сутки в течение месяца продемонстрировал значительное превосходство над плацебо, улучшение данных рН мониторинга пищевода и снижение тяжести симптомов ГЭРБ . Была также отмечена хорошая его переносимость. Препарат ингибирует 34 -60 % спонтанных расслаблении нижнего пищеводного сфинктера и повышает его базальное давление . Однако данных оправдывающее широкое применение баклофена в терапии ГЭРБ еще недостаточно.
Лечебные режимы.
В настоящее время существуют два основных тактических подходов к лечению ГЭРБ, так называемые step-up и step-down. Первый применение наиболее слабых мер (модификация стиля жизни, антациды) в качестве первого этапа лечения с постепенным применением все более мощных препаратов при неэффективности (Н2 блокаторов, затем их сочетание с прокинетиками и только потом PPI). Второй вариант терапии предусматривает назначение наиболее эффективного лечения (PPI), позволяющего быстро купировать симптоматику, а затем снижать дозу лекарств и возможно переходить на более слабые препараты.
В нашей практике мы придерживаемся только step-down терапии т.к. считаем, что пациент обращается к нам для быстрейшего купирования беспокоящих его симптомов, что и должно быть достигнуто назначением группы препаратов, от которой можно ожидать лучшего эффекта. Вы не должны забывать о советах по изменению стиля жизни, но в сочетании с назначением стандартной дозы PPI. Что касается начала лечения с Н2 блокаторов, с последующим переходом, при необходимости, на PPI - вас за это не осудят, но есть ли в этом смысл? Н2 блокаторы имеют не меньшее число вероятных побочных эффектов, их цена не существенно ниже. Оставим их для терапии по требованию и ночных эпизодов рефлюкса. Правда существует весьма небольшая группа пациентов с рефлюкс эзофагитом рефрактерных к терапии ингибиторами протонной помпы у которых достаточный контроль рН может быть достигнуть применением высоких доз Н2 блокаторов .
А как поступать с эндоскопически негативной ГЭРБ? Да точно также. Как было сказано выше, степень морфологических изменений в пищеводе плохо коррелирует с тяжестью симптоматики . Более того, в этой группе больных часто наблюдается менее выраженный эффект от антисекреторной терапии с более длительным сохранением симптомов . Необходимо помнить так же, что эффективность Н2 блокаторов при эндоскопически негативной ГЭРБ не превосходит таковую при эрозивном рефлюкс эзофагите .
При тяжелом рефлюкс-эзофагите (С, D) рациональным является терапия наиболее мощным PPI (нексиумом) или максимальной дозой других ингибиторов протонной помпы.
При ночных эпизодах изжоги не смотря на применений PPI рационально добавить однократный вечерний прием Н2 блокатора. Антациды могут применяться как контролируемая пациентом терапия "по требованию".
Итак, мы придерживаемся сведущей тактики лечения при появлении нового пациента с ГЭРБ.
- Ингибиторы протонной помпы в стандартной дозе (в течении 2-4 недель при эндоскопически негативном рефлюкс-эзофагите и эрозивном эзофагите степени A, B и в течении 8 недель при его более тяжелых формах).
- При неэффективности (определяемой по сохранению симптоматики после 7-10 дней лечения или сохранению эндоскопической картины эзофагита) - повышение дозы PPI до максимальной или переходом на потенциально более эффективный PPI - нексиум.
- При неэффективности - рН мониторирование на фоне лечения. Попытка перехода на высокие дозы Н2 блокаторов в сочетании с прокинетиками? Антирефлюксная операция?
- При эффективности - постепенное снижение дозировки вплоть до отмены препарата. Если симптомы рецидивируют - прием минимально эффективной дозы препарата (возможна терапия через день или терапия выходного дня), обсуждение возможности антирефлюксной операции.
Поддерживающая терапия.
Исходя из хронической природы ГЭРБ существует необходимость поддерживающей терапии. Снижение дозы медикамента или попытка проведения поддерживающей терапии менее мощным, чем использовавшимся для лечения препаратом часто приводит к высокой частоте рецидивов. Только у примерно 20 % пациентов после проведения курсового лечения изменения стиля жизни и периодический прием антацидов достаточны для поддержания ремиссии. Н2 блокаторы и прокинетики малоэффективны для поддержания ремиссии у пациентов у которых она была достигнута с использованием PPI . Наиболее эффективна терапия низкими дозами PPI. Эффективность терапии выходного дня и приема препаратов через день дискутабельна.
Заключение.
Медикаментозная терапия остается основой лечения ГЭРБ. Препаратами выбора в лечении и проведении долговременной поддерживающей терапии являются PPI. Роль Нр инфекции в развитии и естественном течении ГЭРБ, как и ее влияние на исход лечения до конца не ясны. Разработка новых препаратов и сравнение эффективности различных схем их применения является перспективным направлением дальнейшего улучшения качества лечения этой патологии.
Литература
- Пиманов И.С. Эзофагит, гастрит и язвенная болезнь. Н. Новгород 2000.
- Antonson CW, Robinson MG, Hawkins TM, et al. High doses of histamine antagonists do not prevent relapses of peptic esophagitis following therapy with a proton pump inhibitor. Gastroenterology 1990;98:A16.
- Berstad AE, Hatlebakk FG, Maartmann-Moe H, et al. Helicobacter pylori, gastritis and epithelial cell proliferation in patients with reflux oesophagitis after treatment with omeprazole. Gut 1997;41:735-739
- Castell DO, Kahrilas PJ, Richter JE, Vakil NB, Johnson DA, Zuckerman S et al. Esomeprazole (40 mg) compared with lansoprazole (30 mg) on the treatment of erosive esophagitis. Am J Gastroenterol 2002;97:575-83.
- Ciccaglione AF, Bartolacci S, Marzio L. Effects of one month treatment with GABA agonist baclofen on gastro-esophageal reflux and symptoms in patients with gastro-esophageal reflux disease. Gastroenterology. 2002;122:A-196.
- Dent J, et al. An evidence-based appraisal of reflux disease management the Genval Workshop Report. Gut 1998;44(Suppl 2):S1-S16 (April).
- DeVault K, Castell D and The Practice Parameters Committee of the American College of Gastroenterology. Updated Guidelines for the Diagnosis and Treatment of Gastroesophageal Reflux Disease. Am J Gastroenterol 1999;94:1434-1442.
- Fass R. Epidemiology and pathophysiology of symptomatic gastroesophageal reflux disease. Am J Gastroenterol.
- Galmiche JP, Fraitag B, Filoche B, et al. Double-blind comparison of cisapride and cimetidine in treatment of reflux esophagitis. Dig Dis Sci 1990;35:649-55.
- Haruma K, Mihara M, Kawaguchi H, et al. Low prevalence of Helicobacter pylori infection in patients with reflux oesophagitis . Gastroenterology 1996;110:A130.
- Holloway RH. GABA-B receptors and control of gastrointestinal motility. In: AGA Research Symposium: GABA-B receptor agonists as novel treatments of reflux disorders. Program and abstracts of Digestive Disease Week 2002; May 19-22, 2002; San Francisco, California.
- Koehler RE, Weymean PJ, Oakley HF. Single- and double-contrast techniques in esophagitis. AJR 1980;135:15-9.
- Kuipers EJ, Lundell L, Klinkenberg-Knoll EC, et al. Atrophic gastritis and Helicobacter pylori infection in patients with reflux oesophagitis treated with omeprazole or fundoplication. N Engl J Med 1996;334:1018-1022.
- Labenz J, Malfertheiner P. Helicobacter pylori in gastro-oesophageal reflux disease: causal agent, independent or protective factor? Gut 1997;41:277-280.
- Laine L; Sugg J Effect of Helicobacter pylori eradication on development of erosive esophagitis and gastroesophageal reflux disease symptoms: a post hoc analysis of eight double blind prospective studies. Am J Gastroenterol 2002 Dec;97(12):2992-7 (ISSN: 0002-9270).
- Lamberts R, Creutzfeldt W, Struber HG, et al. Long term omeprazole therapy in peptic ulcer disease: gastrin, endocrine cell growth and gastritis. Gastroenterology 1993;104:1356-1370.
- Leite LP, Just RJ, Castell DO, et al. Control of gastric acid with high dose H2-receptor antagonists after omeprazole failure: Report of two cases. Am J Gastroenterol 195;90:1874-7.
- Lepoutre L, Van der Spek P, Vanderlinden I, et al. Healing of grade-II and III oesophagitis through motility stimulation with cisapride. Digestion 1990;45:109-14.
- Lind T, Rydberg L, Kylebдck A, Jonsson A, Andersson T, Hasselgren G et al. Esomeprazole provides improved acid control vs. omeprazole in patients with symptoms of gastro-oesophageal reflux disease. Aliment Pharmacol Ther 2000;14:861-7.
- Lundell L, Havu N, Andersson A, et al. Gastric atrophy development and acid supression therapy revisited. Result of a randomised clinical study with long term follow up . Gastroenterology 1997;112:A28.
- Mann SG, Murakami A, McCarroll K, et al. Low dose famotidine in the prevention of sleep disturbance caused by heartburn after an evening meal. Aliment Pharmacol Ther 1995;9:395-401.
- Ott DJ, Wu WC, Gelfand DW. Reflux esophagitis revisited: Prospective analysis of radiological accuracy. Gastrointest Radiol 1981;6:1-7. Koehler RE, Weymean PJ, Oakley HF. Single- and double-contrast techniques in esophagitis. AJR 1980;135:15-9.
- Ott DJ, Chen YM, Gelfand DW, et al. Analysis of a multiphasic radiographic examination for detecting reflux esophagitis. Gastrointest Radiol 1986;11:1-6.
- Richter JE, Long JF. Cisapride for gastroesophageal reflux disease: A placebo-controlled, double-blind study. Am J Gastroenterol 1995;90:423-30.
- Robinson M, Yale J Biol Med 1999 Mar-Jun;72(2-3):169-72 (ISSN: 0044-0086).
- Rоhss K, Hasselgren G, Hedenstrцm H. Effect of esomeprazole 40 mg vs omeprazole 40 mg on 24-hour intragastric pH in patients with symptoms of gastroesophageal reflux disease. Dig Dis Sci 2002;47:954-8.
- Saco LS, Orlando RC, Levinson SL, et al. Double-blind controlled trial of bethanecol and antacid versus placebo and antacid in the treatment of erosive esophagitis. Gastroenterology 1982;82:1369-73.
- Sehiguchi T, Shirota T, Horikoshi T, et al. Helicobacter pylori infection and severity of reflux oesophagitis . Gastroenterology 1996;110:A755.
- Tew S, Jamieson GG, Pilowski I, et al. The illness behavior of patients with gastroesophageal reflux disease with and without endoscopic esophagitis. Dis Esophagus 1997;10:9-15.
- Vicari JJ, Peek RM, Falk GW, et al. The seroprevalence of cag A-positive Helicobacter pylori strains in the spectrum of gastro-oesophageal reflux disease. Gastroenterology 1998;115:50-57.
- Vigneri S, Termini R, Leandro G, et al. A comparison of five maintenance therapies for reflux esophagitis. N Engl J Med 1995;333:1106-10.
- Werdmuller BFM, Loffeld RJLF. Helicobacter pylori infection has no role in the pathogenesis of reflux esophagitis. Dig Dis Sci 1997;42:103-105. 135.
- Wilder-Smith C, Rцhss K, Lundin C, Rydholm H. Esomeprazole 40 mg provides more effective acid control than pantoprazole 40 mg. J Gastroenterol Hepatol 2002;17 Suppl:A784.
- Wilder-Smith C, Rоhss K, Claar-Nilsson C, Lundin C. Esomeprazole 40 mg provides faster and more effective acid control than lansoprazole 30 mg in patients with symptoms of gastroesophageal reflux disease. Gastroenterology 2002;122 4 Suppl 1:A200.
- Wilder-Smith C, Claar-Nilsson C, Hasselgren G,Rоhss K. Esomeprazole 40 mg provides faster and more effective acid control than rabeprazole 20 mg in
patients with symptoms of GERD. J Gastroenterol Hepatol 2002;17 Suppl:A612.
О том, что нужно питаться правильно, известно всем, но вот придерживаются принципов рационального питания – единицы, остальные мучаются от лишнего веса, проблем с пищеварением или изжоги. Согласно наблюдениям гастроэнтерологов – изжога, которая часто является симптомом гастроэзофагеальной рефлюксной болезни, сегодня становится одной из самых часто встречающихся жалоб при заболеваниях желудочно-кишечного тракта. Большинство больных даже не подозревает о существовании такого заболевания, как ГЭРБ, заедая и запивая изжогу разнообразными продуктами или лекарствами и тем самым только ухудшая ситуацию, а ведь вылечить гастроэзофагеальную рефлюксную болезнь не так уж сложно, главное – вовремя взяться за лечения и не пускать все на самотек.
Что такое ГЭРБ
Гастроэзофагеальная рефлюксная болезнь, рефлюкс эзофагит или ГЭРБ – это хроническое рецидивирующее заболевание пищеварительной системы . В последнее время ученые и клиницисты отмечают рост числа больных ГЭРБ, причем, как правило, заболевшие – это успешные, достаточно молодые люди, проживающие в больших промышленных центрах, крупных городах и ведущие малоподвижный образ жизни. При ГЭРБ кислое содержимое желудка и, реже, двенадцатиперстной кишки, попадает в пищевод, вызывая его раздражение, постепенно слизистая оболочка пищевода воспаляется, на ней образуются очаги эрозии, а затем – язвы. В основе заболевания лежит функциональная недостаточность верхнего желудочного и других клапанов, которые должны удерживать содержимое желудка и не допускать попадание кислоты в вышерасположенные органы. По мнению ученых, ГЭРБ вполне может занять место гастрита среди болезней, спровоцированных образом жизни, так как рост числа заболевших объясняется снижением физической активности людей, вредными привычками и неправильным питанием.
Причины развития гастроэзофагеальной рефлюксной болезни
Чаще всего гастроэзофагеальная рефлюксная болезнь развивается из-за воздействия нескольких факторов сразу. В этиологии ГЭРБ различают причину развития болезни и факторы, способствующие ее появлению.
1. Снижение тонуса кардиального сфинктера – мышечное кольцо, которое должно удерживать кислое содержимое желудка может «расслабиться» из-за переедания, привычки употреблять большое количество напитков, содержащих кофеин, курения, регулярного употребления спиртных напитков, а также из-за длительного применения некоторых лекарственных препаратов, таких как, антагонисты кальция, спазмолитики, НПВС, антихолинэргики, бета адреноблокаторы, антибиотики и другие. Все эти факторы способствуют снижению мышечного тонуса, а курение и алкоголь также увеличивают количество вырабатываемой кислоты;
2. Повышение внутрибрюшного давления – увеличение давления внутри брюшной полости также приводит к тому, что сфинктеры раскрываются и содержимое желудка попадает в пищевод. Повышение внутрибрюшного давления встречается у людей, страдающих от лишнего веса; у больных с асцитом, при заболеваниях почек или сердца; при вздутии кишечника газами и при беременности;
3. Язвенная болезнь желудка и двенадцатиперстной кишки – хеликобактер пилори, чаще всего провоцирующая начало заболевания, также может стать причиной развития ГЭРБ или болезнь появляется при лечении язвы антибиотиками и препаратами, снижающими кислотность желудочного сока;
4. Неправильное питание и неправильное положение тела – чрезмерное употребление жирной, жареной и мясной пищи вызывает усиление секреции желудочного сока, а из-за затрудненного переваривания пища застаивается в желудке. Если же после пищи человек сразу же ложится или его работа связана с постоянными наклонами – риск возникновения ГЭРБ возрастает в несколько раз. Сюда же можно отнести привычку питаться «на бегу» и пристрастие к фаст-фуду – при этом заглатывается много воздуха, а пища в желудок попадает практически не пережеванной и не готовой к перевариванию, в результате, из-за воздуха, давление в желудке возрастает, а переваривание пищи затрудняется. Все это вызывает ослабление пищеводных сфинктеров и постепенно может развиться ГЭРБ;
5. Генетическая предрасположенность – примерно 30-40% всех случаев ГЭРБ обусловлены наследственной предрасположенностью, у таких больных наблюдается генетическая слабость мышечных структур или другие изменения в желудке или пищеводе. При действии 1 или нескольких неблагоприятных факторов, например, переедания или беременности, у них развивается гастроэзофагеальная болезнь;
6. Диафрагмальная грыжа – грыжа пищеводного отверстия диафрагмы образуется, если в отверстие в мембране, где расположен пищевод, попадает верхняя часть желудка. При этом давление в желудке многократно возрастает и это может спровоцировать развитие ГЭРБ. Такая патология чаще всего наблюдается у людей старшего возраста, после 60-65 лет.
Симптомы ГЭРБ
Большинство больных ГЭРБ в начале заболевания даже не подозревают о своей проблеме, симптомы болезни появляются редко, не доставляют особого неудобства и редко правильно диагностируются больными. Так, большинство заболевших считают, что у них нарушение пищеварения, гастрит или язва желудка.
Основные симптомы гастроэзофагеальной болезни
- Изжога или выброс кислого содержимого желудка – основной симптом ГЭРБ. Изжога появляется сразу после или через некоторое время после приема пищи, больной чувствует жжение, распространяющееся от желудка к пищеводу, а при сильных приступах ощущает горечь и неприятный вкус во рту. Приступы изжоги при ГЭРБ не всегда связаны с приемом пищи, они могу возникать, когда больной лежит, ночью, во время сна, при подъемах, наклонах и, особенно, после употребления тяжелой, мясной пищи.
- Синдром диспепсии – встречается примерно у половины больных ГЭРБ, чаще возникает при наличии других заболеваний желудочно-кишечного тракта. При диспепсии больной ощущает боль и тяжесть в области желудка, ощущение переполнения, тошноты после еды, реже возникает рвота кислым или пищей.
- Боль за грудиной – характерный симптом ГЭРБ, помогающий отличить ее от гастрита и язвы. При гастроэзофагеальной рефлюксной болезни из-за раздражения пищевода кислотой у больных возникает чувство сильной боли и жжение за грудиной, иногда боли при ГЭРБ такие интенсивные, что их путают с приступами инфаркта миокарда.
- Симптомы поражения верхних дыхательных путей – реже у больных, из-за постоянного раздражения кислотой голосовых связок и горла возникают такие симптомы, как охриплость голоса и боль в горле; дисфагия – нарушение глотания, при этом больные чувствуют комок в горле, когда глотают или пища «застревает» в пищеводе, вызывая сильную боль в груди. Также при ГЭРБ могут быть стойкая икота, кашель и образование мокроты.
Диагностика ГЭРБ
Диагностика ГЭРБ достаточно сложна, обычно пациенты обращаются за медицинской помощью достаточно поздно, когда заболевание переходит в 3-4 стадию. Диагноз заболевания выставляют на основании клинических признаков: стойкой изжоги, отрыжки кислым и после проведения специальных исследований, позволяющих визуализировать повреждения в пищеводе и нарушение работы верхнего желудочного сфинктера:
- рентгенологическое исследование желудка с применение функциональных проб – позволяет выявить повреждения слизистой оболочки желудка и пищевода, а также нарушение моторики;
- фиброэзофагогастродуоденоскопия (ФГДЭС) – дает возможность врачу визуально оценить степень повреждения слизистой оболочки пищевода;
- пищеводная манометрия – измеряется давление в дистально отделе пищевода, при недостаточности пищеводного сфинктера – давление в желудке и пищеводе практически одинаково;
- тест с ингибитором протоновой помпы – применение омепразола или рабепрозола, уменьшающих выработку соляной кислоты, позволяет выявить наличие или отсутствии ГЭРБ;
При затруднении в диагностики болезни применяют другие, более специфические методы диагностики: импедансометрию, электромиографию, сцинтиграфию, внутрипищеводный рН-мониторинг и другие.
Лечение
В основе лечения неосложненной ГЭРБ, без тяжелых повреждений слизистой оболочки пищевода лежит изменение образа жизни:
- полный отказ от курения и употребления алкогольных напитков;
- изменение рациона питания — отказ от тяжелых, мясных блюд, газированных напитков, кофе, крепкого чая и любых других продуктов, провоцирующих повышенную выработку соляной кислоты;
- изменение режима питания – дробное питание – 5-6 раз в день, небольшими порциями;
- увеличение физической активности;
- нормализация веса;
- отказ от приема таких лекарственных препаратов, таких как нитраты, антагонисты кальция, бета адреноблокаторы и других.
Если больного мучают сильная изжога, боль за грудиной и другие симптомы, ему назначают: препараты, уменьшающие выработку соляной кислоты: ингибиторы протонной помпы (омепразол, рабепрозол), блокаторы Н2–гистаминовых рецепторов (фамотидин), прокинетики (домперидон, мотилиум), антациды (фосфалюгель, гавискон форте).
Также для лечения ГЭРБ используют такие народные средства, такие как отвар льняного семени и другие.
В тяжелых случаях, при неэффективности терапевтических методов и при наличии осложнений: рубцовых сужений пищевода, язв, кровотечений из вен пищевода, проводится хирургическое лечение. В зависимости от тяжести заболевания и наличия осложнений проводят частичное или полное удаление пищевода, фундопликация или расширение пищевода.
Синонимы: гастроэзофагальный рефлюкс, желудочно-пищеводный рефлюкс (ЖПР) . Некорректные наименования: пищеводный рефлюкс, гастро эзофагальный рефлюкс, желудочно пищеводный рефлюкс . Иногда, основываясь на англоязычных традициях, гастроэзофагеальным рефлюксом называют гастроэзофагеальную рефлюксную болезнь (ГЭРБ).
Гастроэзофагеальный рефлюкс у здоровых людей
Гастроэзофагеальный рефлюкс является физиологичным, если он развивается, главным образом, после приёма пищи, не сопровождается дискомфортом, если продолжительность рефлюксов и их частота в течение суток и, особенно ночью, небольшая.В норме, для предупреждения повреждения слизистой оболочки пищевода желудочным содержимым включаются следующие механизмы: барьерная функция гастроэзофагеального соединения и нижнего пищеводного сфинктера, резистентность оболочки пищевода, клиренс пищевода (самоочищение пищевода от частичек пищи, жидкости и рефлюксата).
Нарушения в координации этих механизмов, наличие частых и/или продолжительных эпизодов гастроэзофагеального рефлюкса, особенно в ночное время, возникновение повреждений слизистой оболочки пищевода приводит к развитию гастроэзофагеальной рефлюксной болезни .
Рис.1. рН-грамма пищевода здорового человека с физиологичными гастроэзофагеальными рефлюксами
На рис. 1 дан график кислотности в пищеводе здорового человека, полученный с помощью внутрижелудочной рН-метрии (Рапопорт С.И.). На графике хорошо наблюдаемы гастроэзофагеальные рефлюксы – резкие увеличения кислотности до 2–3 рН (на графике - пики вниз), в данном случае являющиеся физиологичными.
Кислые, слабокислые и щелочные рефлюксы
Результатом большинства желудочно-пищеводных рефлюксов, физиологичных и патологических, является заброс в пищевод кислого желудочного содержимого. Такие рефлюксы являются кислыми . Попадание в пищевод вследствие дуоденогастральных и дуоденогастроэзофагеальных рефлюксов щелочного содержимого двенадцатиперстной кишки, включающего желчные кислоты и лизолецитин могут поднимать pH в пищеводе выше 7. Такие рефлюксы называются щелочными. Хотя эти рефлюксы меньше тревожат пациентов, они представляют большую опасность для здоровья. Если время, в течение которого в пищеводе регистрировалась кислая среда, превышало 4,5 % от общего времени исследования, то есть более часа за сутки, делалось заключение о наличии патологического кислого гастроэзофагального рефлюкса.В 2002 году в Порто (Португалия) была принята классификация, согласно которой рефлюксы, обнаруженные при рН-импедансометрии пищевода, были разделены на кислые рефлюксы (рН < 4), сверхрефлюксы (кислые рефлюксы, возникшие в период осуществления пищеводного клиренса, когда рН в пищеводе еще сохраняется ниже 4), слабокислые - когда уровень рН в пищеводе во время эпизода рефлюкса не опускается ниже 4 (4 < рН < 7) и слабощелочные (рН > 7) (Кайбышева В.О., Сторонова О.А., Трухманов А.С., Ивашкин В.Т.).
Классификация рефлюксов по уровню кислотности *)
Не все исследователи считают правомочным использовать нижний лимит для слабокислых рефлюксов в рН 7. Так, Zerbib F. с соавт. рекомендуют считать рН 6,5 как границу между слабокислым и слабощелочным рефлюксом (Валитова Э.Р., Бор С.).

Рис. 2. Импеданс-рН-метрия пищевода. Показаны 4 типа рефлюксов: (A) слабокислой рефлюкс, (B) кисый рефлюкс, (С) слабощелочной рефлюкс и (D) сверхрефлюкс (Yu Kyung Cho
)
На рис. 3 изображена суточная рН-грамма ребенка с патологическими кислыми рефлюксами ():

Рис. 3. Суточная рН-грамма пищевода ребенка с патологическими кислыми рефлюксами
Подъёмы рН в пищеводе выше 7,5 более 27 раз в сутки расценивались как патологический щелочной гастроэзофагеальный рефлюкс. На рис. 4 дана суточная рН-грамма ребенка с щелочными рефлюксами (Гнусаев С.Ф., Иванова И.И., Апенченко Ю.С.):

Рис. 4. Суточная рН-грамма пищевода ребенка с щелочными рефлюксами
Гастроэзофагальный рефлюкс у детей
В первые три месяца жизни ребенка гастроэзофагеальный рефлюкс характерен и является физиологическим. У детей раннего возраста имеются анатомо-физиологические особенности, предрасполагающие к его развитию. Это недоразвитие дистального отдела пищевода, низкая кислотность желудочного сока, незначительный объём и шарообразная форма желудка, его замедленное опорожнение.Патологический гастроэзофагеальный рефлюкс у детей раннего возраста характеризуется частыми срыгиваниями и рвотой, сопровождающимся недостаточным приростом массы тела, анемией, нарушением общего состояния. Критериями патологичности гастроэзофагеальных рефлюксов у младенцев считается возникновение рефлюкса трёхкратно в течение 5 минут, или если по данным суточной рН-метрии время закисления пищевода менее 4,0 составляет более 8 % общего времени исследования.
Патологический гастроэзофагеальный рефлюкс чаще встречается у недоношенных детей и у новорождённых с патологией головного мозга. Причиной патологического гастроэзофагеального рефлюкса могут быть нарушения регуляции деятельности пищевода со стороны вегетативной нервной системы, чаще всего обусловленные действием повреждающих факторов гипоксически-травматического генеза в период неблагоприятно протекавших беременности и родов. Лёгочная аспирация, вызванная гастроэзофагеальным рефлюксом может быть причиной внезапной смерти у детей раннего возраста, в основе которого лежит центральное апноэ или рефлекторный бронхоспазм (Гнусаев С.Ф., Иванова И.И., Апенченко Ю.С.).
Исследование гастроэзофагеальных рефлюксов
 Наиболее известным проявлением гастроэзофагеальных рефлюксов является изжога - жжение за грудиной, являющаяся результатом воздействия агрессивных компонентов желудочного сока (соляная кислота, пепсин) и попадающих из двенадцатиперстной кишки в желудок вследствие дуоденогастральных рефлюксов желчных кислот , лизолецитина , панкреатических ферментов. Часто ГЭРы происходят ночью, во время сна. Для определения степени патологичности рефлюксов, выявления количественных характеристик уровня воздействия рефлюксата на слизистую оболочку пищевода требуется проведение специальных обследований.
Наиболее известным проявлением гастроэзофагеальных рефлюксов является изжога - жжение за грудиной, являющаяся результатом воздействия агрессивных компонентов желудочного сока (соляная кислота, пепсин) и попадающих из двенадцатиперстной кишки в желудок вследствие дуоденогастральных рефлюксов желчных кислот , лизолецитина , панкреатических ферментов. Часто ГЭРы происходят ночью, во время сна. Для определения степени патологичности рефлюксов, выявления количественных характеристик уровня воздействия рефлюксата на слизистую оболочку пищевода требуется проведение специальных обследований. На первом этапе обычно проводят суточное мониторирование рН пищевода , во время которого устанавливается период времени, в течение которого слизистая оболочка пищевода подвергается воздействию соляной кислоты и оценивается эффективность очистки (клиренса) пищевода от кислого рефлюксата.
Часто причиной рефлюксных заболеваний является неэффективное функционирование нижнего пищеводного сфинктера . Для оценки его запирательной способности и выявления дефектов перистальтики пищевода необходима манометрия пищевода .
Причиной заболеваний пищевода могут быть не только кислые рефлюксы, повреждающими факторами для его слизистой оболочки является желчные кислоты, лизолецитин и т.п. Для исследования такого рода рефлюксов применяется импеданс-рН-метрия пищевода.
Антирефлюксный режим
В связи с тем, что гастроэзофагеальные рефлюксы часто являются причиной заболеваний пищевода и других органов, одним из способов лечения таких болезней является изменение образа жизни, направленное на уменьшение гастроэзофагеальных рефлюксов. Антирефлюксный режим включает:- при наличии излишней массы тела - её снижение
- отказ от курения
- отсутствие физических нагрузок, сопряжённых с наклонами, качанием пресса, поднятием тяжести и других упражнений, повышающих внутрибрюшное давление
- исключение или ограничение потребления продуктов с кислотостимулирующим действием, в частности цитрусов, шоколада, выпечки, свежего белого хлеба, чёрного хлеба, бульонов, специй, грибов, жареной и жирной пищи, редьки, редиса
- отказ от газированных напитков, кофе, крепкого чая, холодной и горячей пищи, переедания
- сон на кровати с приподнятым на 15 см головным концом
- сон не ранее двух часов после еды
- ограничение приёма лекарственных препаратов, усиливающих гастроэзофагеальные рефлюксы.



